ABD'de beş büyük sağlık sistemi, Eisai ve Biogen firmalarının ürettiği, gelecek vadeden yeni Alzheimer ilacı Leqembi'yi, bir ya da iki ay içinde piyasaya sunmaya hazırlanıyor. Yapılan açıklamada ilaç piyasaya sunulmadan önce ödeme, idari süreçler, hastaların izlenmesi gibi konuların ele alınacağı belirtildi.
Geçen ay ABD Gıda ve İlaç Dairesi'nden (FDA) tam onay alan Leqembi, böylece Alzheimer'ın erken evrelerindeki hastalarda hastalığın ilerlemesini yavaşlattığı kanıtlanmış ilk tedavi olmuştu.
Hastalığın, ABD hükümetinin 65 yaş ve üstü için sunduğu sağlık sigortası Medicare kapsamındaki yaklaşık 6,5 milyon kişinin çoğunu etkilediği sanılıyor.
Miami Üniversitesi Miller Tıp Fakültesi Alzheimer araştırma programı başkanı Dr. James Galvin, yeni ilaca olan ilgiyi "Hastalar sıraya giriyor. Tedavi olmak istiyorlar, ancak hemen müdahale etmek zor" sözleriyle aktardı.
İlacı birkaç ay içinde piyasaya sürmeyi planlayanlar arasında Minnesota eyaletinin Rochester kentindeki Mayo Clinic, Chicago'daki Northwestern Memorial Hastanesi ve Los Angeles'taki Cedars-Sinai Hastanesi yer alıyor. Cleveland Clinic ve Utah'ın Intermountain sağlık sistemi ise henüz ilacı sunmaya başlamadıklarını söyledi.
Gıda ve İlaç İdaresi'nin (FDA) onay vermesinin ardından Medicare, ilacın masrafını büyük ölçüde karşılama sözü verdi. Medicare ayrıca tedavi adayları için önerilen beyin görüntüleme yöntemi üzerindeki on yıl sınırlamasını hafifletmeyi düşünüyor.
Wall Street uzmanları Eisai ve ortağı Biogen'in ilacı piyasaya sürmesinin ödeme ve teşhis değerlendirmesindeki sorunlar nedeniyle yavaşlamasını bekliyor.
Merkezi Tokyo'daki Eisai şirketi 2024 yılının Mart ayına kadar 10 bin kişinin ve 2026'ya kadar 100 bin kişinin ilaca erişmesini bekliyor.
Eisai ve Biogen tarafından paylaşılan bir elektronik postada birçok doktorun Leqembi'yi reçete ettiği ve alımın beklendiği gibi ilerlemeye devam ettiği belirtildi.
Dr. James Galvin, bölümündeki beş nörologa düşen 50 veya daha fazla hastanın tedaviyi beklediğini söyledi.
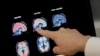
Hastaların tedaviye elverişli olup olmadığı ise çeşitli testler sonucu anlaşılıyor. Bunlar arasında hastaların ilacın etki ettiği erken safhada olduklarından emin olmak için yapılan bilişsel testler, yan etki risklerinin anlaşılması için yapılan genetik testler ve Leqembi'nin mücadele ettiği amiloid adlı proteinin vücuttaki varlığını doğrulamak için yapılan beyin taramaları ile omurilik sıvısı testi yer alıyor.
Galvin, amiloid testinin önemli bir engel gibi göründüğünü söyledi. Hastaneler ve hastalar, daha az invaziv bir test yaklaşımı olan amiloid PET taramalarını tercih ederken Medicare omurilik sıvısı testi için ödeme yapıyor.
Leqembi'nin beyin şişmesi veya kanaması gibi yan etki risklerine karşı hastaların ayrıca tedaviden önce bir kez ve tedavi sırasında birkaç kez MRI taramasına girmesi gerekiyor. Kan pıhtılaşmasını önleyen ilaçların kullanılması da beyinde kanama riskini arttırabilir.
Mayo Clinic doktorlarından David Knopman, beyindeki şişme özellikle hafif olduğunda bunu MRI'da fark etmenin zor olduğunu ve özel eğitim gerektirdiğini söyledi.
Duke Hafıza Bozuklukları Programı Başkanı Dr. Kim Johnson ise 6 Temmuz'da FDA'den tam onay almasından önce, Kuzey Carolina'daki Duke Üniversitesi Sağlık Sistemi'nin ilacı cepten ödeyen 16 hastada kullanmaya başladığını belirtti.
Johnson, sistemin bekleme listesinde 100-150 teşhis edilmiş Medicare hastası olduğunu, ancak bunların tedaviden önce yeniden tetkiklerden geçmeleri gerekeceğini söylüyor.
Pennsylvania Üniversite Hastanesi'nde de klinik uygulamanın bu ay başlaması ve ilk infüzyonun önümüzdeki birkaç gün içinde yapılması bekleniyor.





Forum